NEXUS Magazin: https://www.nexus-magazin.de/artikel/lesen/kuenstlicher-kalkstein-mythos-oder-moeglich
Künstlicher Kalkstein: Mythos oder möglich?
 Man nehme 100 Gramm Kalksteinpulver, ein paar Gramm Kaliumhydroxid-Flocken und etwas Wasser, vermische das Ganze, gieße es in eine Form und warte. Taadaa! Nach einer Woche ist der Kalkstein fertig. Geht nicht? Probieren Sie es. Der Italiener Marcell Fóti war neugierig und hat es getan. Die Ergebnisse seiner Experimente werfen ein neues Licht auf die Steinmonumente der alten Hochkulturen. Wurden die Granit- und Kalksteinblöcke von Pyramide & Co. etwa gegossen? Chemisch ist es definitiv möglich, und auch die Beobachtungen und Messungen vor Ort geben zu denken – wenn sie nicht als Beweis durchgehen. Ist damit ein oft beschworenes Rätsel der Vergangenheit gelöst?
Man nehme 100 Gramm Kalksteinpulver, ein paar Gramm Kaliumhydroxid-Flocken und etwas Wasser, vermische das Ganze, gieße es in eine Form und warte. Taadaa! Nach einer Woche ist der Kalkstein fertig. Geht nicht? Probieren Sie es. Der Italiener Marcell Fóti war neugierig und hat es getan. Die Ergebnisse seiner Experimente werfen ein neues Licht auf die Steinmonumente der alten Hochkulturen. Wurden die Granit- und Kalksteinblöcke von Pyramide & Co. etwa gegossen? Chemisch ist es definitiv möglich, und auch die Beobachtungen und Messungen vor Ort geben zu denken – wenn sie nicht als Beweis durchgehen. Ist damit ein oft beschworenes Rätsel der Vergangenheit gelöst?
Steine ließen sich zu keinem Zeitpunkt in der Geschichte der Menschheit ohne Zuhilfenahme von Bindemitteln künstlich herstellen, das ist hinlänglich bekannt. Und doch bin ich neulich bei meinen Recherchen in Split – genauer gesagt im Keller des Diokletianspalastes – auf einen echten künstlichen Stein gestoßen. Die Beweise dafür möchte ich in diesem Artikel erläutern.
Der Ort des Geschehens liegt also in Split, Kroatien. Falls es Sie einmal dorthin verschlagen sollte, können Sie sich persönlich von meinen Beobachtungen überzeugen. Der Keller ist für Touristen zugänglich, und für gerade einmal acht Euro kann man dieses kleine Wunder bestaunen–obwohl nichts darauf hinweist, dass es sich hierbei um ein Wunder handelt. Kein Schild, keine Pfeile, nichts. Wozu sollte man auch die Aufmerksamkeit der Besucher auf ein simples Stück Kalkstein lenken?
Nun, es handelt sich dabei eben nicht um irgendeinen Kalkstein, sondern um einen künstlichen, von Menschenhand geschaffenen. Was doch eigentlich unmöglich sein sollte – oder etwa nicht?
Ich möchte Sie dazu einladen, meinen Gedankengängen zu folgen. Vielleicht ist es ja doch möglich. Vielleicht habe ich so etwas sogar in meinem eigenen Garten nachgebaut – mit greifbaren Ergebnissen.
Und ja, das Rezept teile ich gerne mit der Welt. Damit auch Sie in Ihrem eigenen Zuhause Wunder vollbringen können.
Aber zunächst Butter bei die Fische: Der kleine Türsturz im Diokletianspalast in Abbildung 1 ist aus künstlichem Kalkstein gemacht.

Abb. 1: Türsturz aus Kalkstein im Diokletianspalast, Split (Bild: Fóti)
Woher ich das weiß? Ganz einfach: Die Risse verraten es. Das sind nicht die üblichen Spannungsrisse, die durch Belastung entstehen (dieser Stein wird nämlich kaum belastet – er liegt ja über einem Hohlraum), sondern, gut aufgepasst: sogenannte Schrumpfrisse durch Austrocknung, auch Trockenrisse genannt.
Und genau die kommen bei natürlichem Kalkstein gar nicht vor. Kalkstein saugt kein Wasser auf, er wird nicht matschig und weich wie Lehm und demzufolge auch nicht wieder trocken und rissig. So ein Kalkstein existiert nicht, schon gar nicht im Dinarischen Gebirge, aus dem dieses Baumaterial stammt.
Dass Kalkstein sich anders als Lehm verhält, sieht man unter anderem an den unzähligen riesigen römischen Wasserzisternen, die genau deshalb aus Kalkstein errichtet wurden, weil er wasserdicht ist. Auch Istanbul ist voll von solchen monumentalen und wunderschönen römischen Kalksteinzisternen, die allein schon einen Besuch wert sind.
An dieser Stelle kommt dann oft der übliche Einwand: „Ja, ja, aber das ist bestimmt nur eine dünne Schicht obendrauf, eine spätere Ausbesserung …“ Nein, ist es nicht. Aber selbst wenn – dann wäre doch das genau der Punkt: Irgendjemand muss irgendwann diesen Stein mit einer künstlichen Kalksteinschicht überzogen haben. Was ebenfalls unmöglich sein sollte.
„Dann kam der Stein eben schon so aus dem Steinbruch. Mit Rissen“, würde der durchschnittliche Archäologe erwidern.
Na schön, von mir aus. Sagen wir, dieser Kalkstein ist nach seiner Entstehung auf dem Meeresgrund zu früh – also noch im weichen Zustand – an Land gelangt und genau dort erhärtet. Für eine solche Rissbildung muss das Material austrocknen, daran ist nicht zu rütteln. Also wurde der Stein vor ein paar Millionen Jahren weich ans Ufer gespült. Das kommt doch schon mal vor, oder?
Nein, tut es nicht.
Schauen wir uns den Stein des Anstoßes doch einmal von unten an – nämlich in Abbildung 2.
Nicht vergessen: Wir sprechen hier von einem Türsturz – also einem Stein, der über eine Türöffnung gelegt wurde. Und jetzt kommt die Eine-Million-Euro-Frage. Bereit?
Gibt es irgendeinen königlichen Steinmetz mit einem Funken Verstand, der einen derart miserablen, komplett rissigen Stein in einem Türsturz verbauen würde?
Hier sollte jeder ohne Publikums- oder Telefonjoker alles darauf setzen, dass die Wahrscheinlichkeit für diesen Fall exakt null Komma null Prozent beträgt.
Wenn Sie wirklich glauben, dass man aus allen verfügbaren Steinen ausgerechnet den schlechtesten genommen und in einem Palast verbaut hat, dann lesen Sie am besten gar nicht weiter. Vergebliche Liebesmüh.
Wenn wir davon ausgehen, dass ein verantwortungsvoller Steinmetz so etwas niemals tun würde, bleibt allerdings nur eine einzige logische Möglichkeit: Der Türsturz war beim Einbau völlig intakt und frei von Rissen. Daraus folgt unweigerlich: Die Risse sind erst später entstanden, nach dem Einbau, durch Schrumpfung beim Austrocknen. Und das ist bei natürlichem Kalkstein schlichtweg unmöglich.
Schachmatt. Was wir hier auf den Bildern sehen, muss ein Türsturz aus künstlichem Kalkstein sein, also aus einer Art uraltem Kalksteinbeton. Eine andere Erklärung ergibt keinen Sinn.
Aber wie ist das möglich? Künstliche Steine? Gibt es nicht, das würde jeder Experte und Archäologe felsenfest behaupten. Punkt.
Eine Einführung in die Welt der künstlichen Steine
Das sieht Joseph Davidovits, Erfinder künstlicher Steine und führender Wissenschaftler auf diesem Gebiet, der nun schon seit einem halben Jahrhundert an zementfreien Materialien forscht (sogenannten Geopolymeren, die den üblichen Beton ersetzen könnten), allerdings etwas anders.

Abb. 2: Schrumpfrisse im Kalkstein (Bild: Fóti)
In Wahrheit ist künstlicher Stein nicht nur realisierbar, es gibt sogar mehr funktionierende Rezepte dafür als Sterne am Himmel. Wenn man es sich genau überlegt, kann es gar nicht anders sein. WasistStein denn eigentlich? Ein chemischer, bei Raumtemperatur fester Stoff. Warum sollte es nicht Abermilliarden verschiedener künstlicher chemischer Stoffe geben, die bei Raumtemperatur hart – vielleicht sogar sehr hart – sind?
Natürlich gibt es sie. Wir nennen sie nur nicht „Stein“, sondern zum Beispiel Glas, Keramik, Metall, Eis oder Würfelzucker. Gut, Würfelzucker ist nicht sonderlich wasserfest, und Eis hat ausgerechnet bei Raumtemperatur den falschen Aggregatzustand – aber das ist eine Frage der Praktikabilität, nicht des Konzepts an sich.
Zwischen bei Raumtemperatur festen Stoffen und sogenannten Steinen gibt es keinerlei fundamentalen Unterschied. Es sind einfach unterschiedliche Moleküle, die in irgendeinem dreidimensionalen Raum starr herumstehen.
Können wir einen solchen Stoff also selbst herstellen? Durchaus. Mehr noch: Davidovits hat festgestellt, dass man solche Materialien sogar aus völlig alltäglichen Substanzen zusammenmischen kann – aus Dingen, die auch den Steinmetzen in der Antike bereits zur Verfügung standen. Es ist also möglich, dass sie daraus betonartige Pampe zusammengerührt und verbaut haben.
Den ersten künstlichen Stein dieser Art hat Davidovits mit seinem Team vor über 20 Jahren angerührt, ausgehend von der simplen (aber wahren) Beobachtung, dass die Kalksteinblöcke der Cheopspyramide in Gizeh Salz enthalten müssen – da sie salzig schmecken. Also stellten sie selbst mehrere Tonnen schwere Kalksteinblöcke her, die bis heute Wind und Wetter trotzen. Menschengemacht. Haltbar.
„Natürlich ist da Salz drin, der Stein ist ja auf dem Meeresboden entstanden“, könnte der gut informierte Nörgler nun erwidern. Aber leider liegt er falsch. Zwar entsteht Kalkstein tatsächlich auf dem Meeresboden, aber Salz ist darin trotzdem nicht enthalten. Wollen Sie sich selbst davon überzeugen? Dann spazieren Sie einfach mal zu einer beliebigen mittelalterlichen Kathedrale und lecken Sie an der Wand. Schmeckt nicht salzig.

Abb. 3: Zufälliger künstlicher Kalkstein (Bild: Fóti)

Abb. 4: Kalksteinanzucht im Selbstversuch (Bild: Fóti)
Wissenschaftlich lässt sich das leicht erklären: Kalkstein, der sich am Meeresgrund ablagert, enthält kein Salz, weil Kochsalz (Natriumchlorid) extrem gut wasserlöslich ist. Es trennt sich nicht einfach so vom Wasser, sondern wird von diesem fortgetragen. Davon kann man sich auch direkt am Strand überzeugen, egal wo auf der Welt. Schauen Sie sich Felsen, Boote oder Hafenmauern an: nirgendwo Salzkrusten. Salz trennt sich nur unter Zwang vom Wasser – durch Verdunstung in Salinen zum Beispiel. Anders geht es nicht.
Ja, gut – das Tote Meer. Dort gibt es hier und dort Salzablagerungen. Aber das ist eben auch eine gigantische Saline – kein normales Meer!
Dasselbe gilt übrigens auch für Kaliumverbindungen: Auch die sind viel zu wasserlöslich, um sich auf dem Meeresboden abzulagern und im Kalkstein zu landen. Dieses Wissen brauchen wir später noch.
Zurück zu Davidovits’ Rezept: Der springende Punkt ist, dass das Salz in den Pyramidensteinen nicht von außen stammt, sondern sich durch die chemische Reaktion der Ausgangsstoffe im Inneren gebildet hat. Davidovits hat eine recht komplexe Formel veröffentlicht, und wer diese befolgt, erhält am Ende einen künstlichen Stein, der chemisch identisch ist mit den inneren Steinblöcken der Cheopspyramide.

Einer der verwendeten Stoffe ist Natron – ein natürliches Salz, das die alten Ägypter für alles Mögliche nutzten, von der Zahnreinigung bis hin zum Mumifizieren. Dieses Natron bildet in Kombination mit Kalkerde (Calciumoxid) eine Art geopolymerartige Bindung im Kalksteinpulver, die das Ganze wieder zu einem festen Kalksteinblock zusammenfügt.
„Aber künstlichen Kalkstein gibt es doch gar nicht wegen Meeresboden, Druck, Millionen Jahren und bla, bla, bla …“
Kurioserweise stimmt das sogar. Den exakt gleichen Stein kann man unter Oberflächenbedingungen tatsächlich nicht nachbauen. Aber darum geht es ja auch nicht. Es ist nicht derselbe Stein, sondern ein chemisch neu zusammengeklebter Kalkstein. Und das „Kleben“ übernimmt dabei das während der Reaktion entstehende Natriumhydroxid, das – wie gesagt – einen neuen Stoff schafft: ein Kalkstein-Geopolymer. Ja, so etwas existiert. Es lässt sich analysieren, messen, aufschlüsseln. Das eigentlich unmögliche Salz im Pyramidenstein.
Nein, das lässt sich nicht auf eine Überschwemmung zurückführen. Kein Hochwasser dieser Welt könnte mit dem Meer konkurrieren, unter dem der Kalkstein Abermillionen Jahre lag, ohne auch nur ein bisschen Salz aufzunehmen. Man könnte die Pyramiden mit so viel Salzwasser übergießen, wie man wollte – kein äußerer Einfluss würde den Kalkstein salzig werden lassen.
Wie haben unsere Vorfahren das Rezept für Kalkstein entdeckt?
Nachdem ich mich mit Davidovits’ Rezept auseinandergesetzt hatte, begann ich mich zu fragen: Wie waren die alten Ägypter auf eine derart komplexe Formel gekommen? Schließlich handelt es sich dabei um einen relativ komplexen Prozess, mindestens auf Niveau der Schulchemie! Dafür ist schon ein beachtlicher Wissensstand vonnöten.
Nach langem Grübeln kam ich zu folgendem Schluss: Wie hat die Menschheit den Wein entdeckt? Durch Zufall. Reinen Zufall. Irgendwann ließ irgendjemand irgendwo eine Schale mit Früchten stehen, die vor sich hin goren, eine Frau verfütterte das vergorene Zeug an ihre Hühner und die fingen an, wie betrunkene Matrosen herumzueiern. „Na, so was“, dachte sich der Mensch. „So torkeln will ich auch!“
Aus diesem ersten Zufall entwickelte sich über Jahrhunderte hinweg durch bewusstes Probieren und Herumexperimentieren eine mehr oder weniger systematische Weinkultur mit Holzfässern, Weinkellern usw. Das Wissen, wie genau all das funktioniert, bewegte sich jedoch weiterhin auf einem ziemlich infantilen Niveau.
Der Bauer wusste nicht, dass die Gärung durch Hefepilze verursacht wird, er wusste nicht, dass beim Gären durch die Bildung von CO2giftige Gase entstehen, und er war felsenfest überzeugt, dass er dem „Kellergeist“ seinen Erfolg verdankte. Heute wissen wir natürlich, dass einfach konstante 16 Grad Celsius den kleinen, aber feinen Unterschied ausmachen. Keine esoterischen Kellergeister, nur reine Physik. Der beste Beweis dafür sind unsere heutigen hochmodernen Weingüter mit Gärtanks aus Edelstahl und Kühlsystemen, die sich kaum stärker von den damaligen Kellerhöhlen unterscheiden könnten.
Aber zurück zu den Steinen.
Die Sache ist: In den zigtausend Jahren unserer Menschheitsgeschichte besitzen wir gerade einmal seit 50 bis 60 Jahren das wissenschaftliche Know-how, um wirklich zu verstehen, was einen guten Wein ausmacht – abgesehen von guten Trauben natürlich. Trotzdem wurde in all den Jahrtausenden zuvor schon hervorragender Wein hergestellt – quasi im Blindflug, nur durch Erfahrung und Ausprobieren.
Und genau so ist es auch mit dem künstlichen Stein. Sie fragen sich jetzt bestimmt: Wie kann man so etwas wie einen geopolymerartigen, neu verklebten Kalkstein zufällig entdecken?
Seit Jahrtausenden benutzen wir Menschen Feuer. Schon damals, als wir noch unter freiem Himmel lebten, weshalb unsere Vorfahren quasi überall Feuer gemacht haben: auf fruchtbarem Boden (im Wald), auf felsigem Untergrund (zum Beispiel in einer Kalksteinhöhle) und auch auf Berggipfeln (sagen wir mal: Granit).

Abb. 5: Selbst hergestellter Block aus künstlichem (also „unmöglichem“) Kalkstein (Bild: Fóti)

Abb. 6: Kalkstein mit Abdrücken (Bild: Fóti)
Da es in diesem Artikel aber um künstlichen (also „gefälschten“) Kalkstein geht, bleiben wir bei den Feuern, die auf kalksteinhaltigem Boden entzündet wurden.
Kleiner Exkurs: Unser Planet ist verdammt alt. Ungefähr vier Milliarden Jahre. Da überrascht es kaum, dass die meisten Gesteine auf der Erde ziemlich zerbrochen oder sogar ganz zerbröselt sind. Die meisten gehen zwar davon aus, dass in Steinbrüchen schöne Platten aus Granit, Marmor oder Kalkstein abgebaut werden – in Wirklichkeit aber gewinnt man in 95 Prozent der Steinbrüche vor allem Schutt und Staub, weil es eben das ist, was es dort gibt. Kein Witz, das lässt sich leicht nachprüfen.
Was ich damit sagen will: Wenn Sie jetzt glauben, dass das, was ich Ihnen erzählt habe, nicht stimmen könnte, weil man ja zuerst das seltene Steinpulver künstlich herstellen müsse, dann sind Sie auf dem Holzweg. Im Gegenteil: Große,intakte Steinblöcke sind ein wirklich seltenes Gut, nach dem man gezielt suchen muss. Ja, im Dinarischen Gebirge gibt es eine Menge davon, aber das gilt eben nicht für alle Gegenden. Steinpulver hingegen liegt überall herum. Man stolpert förmlich darüber, wirbelt es auf, und mancherorts gibt es so viel davon, dass man gar nicht weiß, wohin damit.

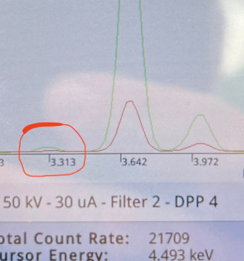
Abb. 7: RFA-Handspektrometer im Einsatz. Rechts die Ergebnisse der Türsturzmessung. (Bild: Fóti)
Zurück zum Thema: Unsere Vorfahren machen also auf einem natürlichen, von Kalksteinbruchstücken und mit Kalkpulver durchsetzten Boden ein Feuer. Dafür nehmen sie natürlich Holz, das abbrennt. Was übrig bleibt, ist Asche. Und nun?
Jetzt kommt der Regen ins Spiel. Das Regenwasser wäscht die wasserlöslichen Bestandteile der Asche aus – vor allem zwei der üblichen Verdächtigen: Kalium- und Natriumverbindungen. Kalium kommt als essenzielles Spurenelement für den Pflanzenstoffwechsel in allen Pflanzen vor. Natrium hingegen findet sich nur in salztoleranten Pflanzen – das lassen wir jetzt mal außen vor.
Wenn das Regenwasser mit Kaliumoxid aus der Asche in Berührung kommt, entsteht Kaliumhydroxid (KOH). Und bei Kaliumhydroxid handelt es sich um eine starke Lauge – nichts, worin man ohne Handschuhe herumwühlen sollte. Seifensieder, die Asche auslaugen, wissen nur zu gut, dass es aus allem Seife macht.
Und wie sein naher Verwandter Natriumhydroxid ist auch Kaliumhydroxid ein bekanntes geopolymerbildendes Mittel.
Jetzt fehlt nur noch ein nicht ganz trivialer Schritt, den ich vorhin bei meinem Bericht über die Pyramidensteine ein wenig vernachlässigt habe: Wie genau bildet die Lauge aus Kalksteinpulver ein Geopolymer? Durch die sogenannte Zementation.
Tatsächlich enthält Kalkstein immer irgendwelche Verunreinigungen – und genau die sorgen dafür, dass aus Pulver überhaupt ein Stein wird. Wenn ein Kalkstein völlig rein ist, dann ist er gleichzeitig weich. Erst die Verunreinigungen machen ihn hart.
Und Kaliumhydroxid (sowie Natriumhydroxid) löst genau diese Verunreinigungen auf und bindet sie neu – es „zementiert“ das Kalkpulver also erneut zu einer festen Masse.
Was passiert nun nach dem ersten Regen? Erst einmal noch nicht viel. Aber ein bisschen Kaliumhydroxid sickert bereits aus der Asche ins Kalksteinpulver, und dort wird langsam der Zementationsprozess in Gang gesetzt. Noch nichts Spektakuläres.
Unsere Vorfahren machen wieder Feuer an derselben Stelle, das brennt wieder nieder – dann kommt wieder der Regen. Noch mehr Kaliumhydroxid sickert ins Kalksteinpulver. Wenn das sechs- bis achtmal passiert, bildet sich unter der Feuerstelle eine feste Kalksteinschicht – eine Art „Kalkstein-Pfannkuchen“. Das Kalkpulver ist wieder zu einem festen Ganzen zusammengewachsen.
Und jetzt trennt uns nur noch ein kleiner Schritt zum gezielten Experimentieren mit künstlichem Kalkstein. Woher kommt dieser seltsame Pfannkuchen unter der Feuerstelle? Wer hat ihn dort hingelegt? Niemand? Dann ist er vielleicht direkt dort entstanden? Aber wie? Und woraus?
Ich bin übrigens selbst über unzählige Wanderwege durch den Wald gezogen und habe unter alten Feuerstellen nach solchen Kalksteinpfannkuchen gesucht – und bin tatsächlich fündig geworden! Dieses Phänomen tritt auch heute noch auf: Wenn es auf Asche regnet, löst sich Kaliumhydroxid und sickert in Richtung Erdmittelpunkt.
In Abbildung 3 ist ein wunderschönes Exemplar eines solchen künstlichen Kalksteins, das ich tief unter der Asche in einem nahen kleinen Waldstück gefunden habe. Sieht doch aus wie ein Hundehaufen, oder? Ist aber keiner!
Ich selbst glaube ohne Beweise ja grundsätzlich nichts und niemandem, nicht einmal mir selbst. Und das sollten Sie auch nicht, solange ich nicht langsam mit Beweisen um die Ecke komme.
Also aufgepasst! Ich versuche gerade unter Laborbedingungen, mit dem oben beschriebenen Verfahren (Kalksteinpulver, darauf Asche, darauf Regen) künstlichen Kalkstein herzustellen. Die sechs kleinen Becher in Abbildung 4 habe ich alle zur Hälfte mit Kalksteinpulver und zur Hälfte mit Asche gefüllt und dann ordentlich mit Wasser durchtränkt. In diesem Experiment werde ich es insgesamt sechsmal „regnen“ lassen.
Nach jedem „Regen“ lasse ich das Ganze erst einmal gut durchtrocknen, damit sich alles verbinden kann, was sich verbinden will. Pro Runde opfere ich einen Probenbecher: Ich nehme das kleine Kalksteinstück vom Boden des Bechers und teste seinen Härtegrad. Nach dem sechsten Regen werden meine Becher dann aufgebraucht sein.
Das Experiment ist noch nicht abgeschlossen – bisher habe ich es zweimal „regnen“ lassen –, aber eines kann ich jetzt schon sicher sagen: Bereits nach dem ersten Regen hat sich das Kalksteinpulver zu einer Art härterer Pampe verbunden. Noch kein Stein, aber deswegen habe ich ja sechs Becher: damit es sechsmal regnen kann.
Genau genommen ist das Experiment überflüssig, denn ich weiß bereits, dass Kalksteinpulver sich mit Kaliumhydroxidlösung zu einem festen Stein verbindet – ich habe es schon mehrfach ausprobiert. Mit meinem Becherversuch möchte ich lediglich überprüfen, ob man künstlichen Kalkstein auch völlig zufällig entdecken könnte.
Die Jahreszahl in meinem selbst hergestellten Kalksteinblock (siehe Abbildung 5 und das Rezept) habe ich mit einem Kupfermeißel eingeritzt und anschließend mit geschmolzenem Kupfer ausgegossen. Kleiner Scherz am Rande: Das sind nur Geburtstagskerzen mit abgeschnittenem Docht, die ich in das weiche Material gepresst habe. Die drei Pflastersteine habe ich deshalb draufgelegt, um zu testen, ob sie Spuren auf der Oberfläche hinterlassen. Denn an vielen Orten auf der Welt sieht die Oberfläche von gegossenem Kalkstein so aus wie in Abbildung 6.
Wenn man beim Trocknen nicht geduldig genug ist, bekommt man ein solches Ergebnis. Das Foto in Abbildung 6 habe ich auf dem Dach des Tempels von Dendera in Ägypten fotografiert – ein klassisches Beispiel für die Verwendung von gegossenem Kunstkalkstein.
Aber widmen wir uns nun wieder unserem Türsturz aus Kroatien. Bislang sagen uns ja nur Logik und gesunder Menschenverstand, dass er aus künstlichem Kalkstein besteht. Doch das reicht nicht. Wo bleibt der wissenschaftliche Beweis?
Glücklicherweise war ich genau deshalb nach Split gereist, um diesen wissenschaftlichen Beweis zu erbringen. Zu dem Zweck hatte ich ein spezielles Gerät dabei: ein sogenanntes Röntgenfluoreszenz-Handspektrometer. Dieses beschießt das zu analysierende Material mit Elektronen, und die Atome im Material senden je nach Element ein Signal auf einer bestimmten Frequenz zurück, das sagt: „Hier bin ich!“
Ein lustiges Gerät, dieses überdimensionierte Fieberthermometer, denn es lügt, dass sich die Balken biegen. Man muss höllisch aufpassen, wenn man damit wirklich finden will, wonach man sucht. Natürlich lügt es nicht aus Bosheit, sondern weil es genau das, was wir von ihm wollen, eben nicht direkt kann und das gewünschte Ergebnis notfalls eigenmächtig „erfindet“.


Abb. 8: Kalksteine im Diokletianspalast. Links: kein Kalium, rechts: kaliumhaltig. (Bild: Fóti)
Ein Beispiel: Wir würden gern die prozentuale Zusammensetzung der Bestandteile unseres Steins sehen. Das Gerät misst aber lediglich, wie viele Röntgenstrahlen zurückkommen. „Hier haben wir 1.352 Signale auf der Frequenz von Kalium.“
Aber ich will es jetzt gar nicht zu kompliziert machen. Wichtig ist nur: Wenn jemand wie Sie oder ich Kalium in Gestein finden will, kann er die tolle Gerätesoftware, die ganzen aufgehübschten Tabellen und Kreisdiagramme getrost vergessen. Man muss sich direkt die Rohdaten anschauen. Sonst kommt man nämlich wie sämtliche Archäologen bisher zu dem Schluss: „In diesem Türsturz ist kein fremder Stoff enthalten.“
Aber wissen Sie was? Den gibt es doch!
Und zwar Kalium. Ätsch!
An der rot eingekreisten Stelle (Abb. 7, rechts) ruft das Kalium bei einer Energie von 3,31 keV laut und deutlich: „Kuckuck!“
Die genaue Menge hat es nicht mehr aufs Bild geschafft, ist aber im Grunde auch nicht weiter wichtig. Kalium im Kalkstein ist schlichtweg ein Ding der Unmöglichkeit (Stichwort Entstehungsbedingungen, Löslichkeitsregeln usw.).Wenn in diesem Stein also Kalium enthalten ist, dann wurde es von Menschenhand hineingebracht.
Wir haben es hier also mit einem künstlichen Kalkstein-Türsturz zu tun, der Kalium enthält – höchstwahrscheinlich in Form von Kaliumhydroxid, also Kalium aus Holzaschelauge. Es ist ein menschengemachter Kalkstein, ein Geopolymer.
Ich überspringe jetzt den Teil meiner Nachforschungen, ob nicht vielleicht irgendwann jemand diesen Stein mit Kaliumseife abgewaschen hat, um uns an der Nase herumzuführen – also ob wir es nicht doch einfach mit einer oberflächlichen Kaliumverunreinigung zu tun haben und ich mich gerade komplett lächerlich mache.
Aber nein, natürlich hat das niemand getan. (Nicht, wenn er nach den UNESCO-Restaurierungsrichtlinien arbeitet, nicht während Vicko Andris Restaurierungsarbeiten im 19. Jahrhundert usw.)
Selbst wenn ich mich irren sollte, würde ich es durchaus verkraften. Wer nicht arbeitet, macht auch keine Fehler.
Aber nein, dieser Stein wurde nicht mit Kaliumseife behandelt. Und selbst wenn, dann nur stellenweise. Denn dann müssen in diesem Kellerraum einige Steine gewaschen worden sein (die Kalium enthalten), andere wiederum nicht (bei denen kein Kalium nachweisbar ist).
Auf den ersten Blick wirkt das alles völlig willkürlich. Manche Steine in diesem Keller enthalten Kalium, andere nicht. Leider hatte ich nicht genug Zeit vor Ort, um das Muster zu entschlüsseln, weshalb ich zum Abschluss zwei typische Exemplare zeige – eins mit Kalium, eins ohne.
Das Erstaunliche daran: Die beiden Steine liegen nur etwa einen Meter voneinander entfernt. Es ist also nicht so, als befänden sich alle kaliumhaltigen Steine in der einen Ecke und alle kaliumfreien in der anderen. Wir haben es hier mit einer Mischmauer zu tun.
Schauen wir uns das erste Exemplar an (Abb. 8, links): Wenn Sie vermuten, dass dieser SteinkeinKalium enthält, liegen Sie goldrichtig. Überall auf der Oberfläche sind deutliche Meißelspuren zu erkennen, der Stein wurde also eindeutig gemeißelt, nicht gegossen. Und wenn er gemeißelt wurde, dann besteht er aus natürlichem, viele Millionen Jahre altem Kalkstein, in dem kein Kalium enthalten sein kann.
Wenig überraschend zeigte die Messung: kein Kalium enthalten!
Aber nur zwei Steinreihen darüber …
Nanu? Wo sind denn hier (Abb. 8, rechts) die Meißelspuren? Es gibt keine. Stattdessen sieht man Bläschen, Schlieren – und natürlich einen riesigen, tiefen Trocknungsriss unten rechts in der Ecke.
Und ja, in diesem Stein ist Kalium enthalten. Ich habe selbst nachgemessen.
Ja, klar, das sind natürlich keine Bläschen, sondern fossile Einschlüsse. Von mir aus. Spielt keine Rolle. Wenn man Kalkbruchstücke zu irgendeinem Brei zusammenrührt, können da ganz locker Fossilien mit im Spiel sein, sofern niemand sie zuvor herausgesiebt hat.
Zu welcher Schlussfolgerung gelangen wir denn nun? Wir haben einen Palastkeller voller seltsamer, angeblich „unmöglicher“ Kalksteine (mit Schrumpfrissen, Kaliumgehalt usw.). Und meine Geschichte steht der offiziellen Lehrmeinung, dass es sich hier durchweg um natürlichen, behauenen Kalkstein handeln muss, diametral gegenüber.
Also … wer hat recht?
Leider ist das meistens der, der am lautesten schreit. Beweise? Wen jucken die schon!
Aber wenn es mir gelingt, den Chor der „Künstlichen Kalkstein gibt es nicht!“-Krakeeler zu übertönen, dann besteht vielleicht die Chance, dass wir der Wahrheit ein Stück näher kommen. Wenn nicht … dann bleibt wohl alles, wie es ist.
Aber vielleicht habe ich ja genau deswegen diesen Artikel geschrieben: Um dem künstlichen Kalkstein eine Stimme zu geben.
Hinweis in eigener Sache
Diesen Artikel habe ich extra für Sie geschrieben – für die Leser des deutschen NEXUS-Magazins. In meinem auf Englisch erschienenen Buch „The Natron Theory“ gehe ich ausführlich auf alle hier angeschnittenen Fragen und Experimente ein – inklusive einfach nachzumachender Rezepte für künstlichen Granit und die sogenannten Inkasteine. Die wurden übrigens (wie viele andere „Gesteine“) auf wundersame Weise 600 bis 800 Kilometer von ihrem vermeintlichen Ursprungsort entfernt verbaut … was mit ziemlicher Sicherheit bedeutet, dass sie eben nicht von dort stammen.

Diese Website verwendet Cookies von Google Analytics, sofern Sie zustimmen.
Weitere Informationen finden Sie in unserer
Datenschutzerklärung.
 Man nehme 100 Gramm Kalksteinpulver, ein paar Gramm Kaliumhydroxid-Flocken und etwas Wasser, vermische das Ganze, gieße es in eine Form und warte. Taadaa! Nach einer Woche ist der Kalkstein fertig. Geht nicht? Probieren Sie es. Der Italiener Marcell Fóti war neugierig und hat es getan. Die Ergebnisse seiner Experimente werfen ein neues Licht auf die Steinmonumente der alten Hochkulturen. Wurden die Granit- und Kalksteinblöcke von Pyramide & Co. etwa gegossen? Chemisch ist es definitiv möglich, und auch die Beobachtungen und Messungen vor Ort geben zu denken – wenn sie nicht als Beweis durchgehen. Ist damit ein oft beschworenes Rätsel der Vergangenheit gelöst?
Man nehme 100 Gramm Kalksteinpulver, ein paar Gramm Kaliumhydroxid-Flocken und etwas Wasser, vermische das Ganze, gieße es in eine Form und warte. Taadaa! Nach einer Woche ist der Kalkstein fertig. Geht nicht? Probieren Sie es. Der Italiener Marcell Fóti war neugierig und hat es getan. Die Ergebnisse seiner Experimente werfen ein neues Licht auf die Steinmonumente der alten Hochkulturen. Wurden die Granit- und Kalksteinblöcke von Pyramide & Co. etwa gegossen? Chemisch ist es definitiv möglich, und auch die Beobachtungen und Messungen vor Ort geben zu denken – wenn sie nicht als Beweis durchgehen. Ist damit ein oft beschworenes Rätsel der Vergangenheit gelöst?










